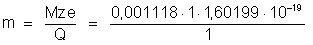As massas dos
átomos săo muito pequenas, da ordem de milésimo de bilionésimo de
bilionésimo de grama. Portanto, năo podem ser medidas por pesagens
comuns. Săo medidas por processos indiretos. A eletrólise fornece
um desses processos. Para determinarmos a massa do átomo de um
elemento, fazemos eletrólise de um ácido, base ou sal em cuja composiçăo
entre o elemento. Seja:
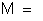 massa do elemento depositada em um dos eletrodos;
massa do elemento depositada em um dos eletrodos;
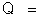 carga elétrica que passa pela soluçăo durante a eletrólise
(
carga elétrica que passa pela soluçăo durante a eletrólise
(
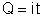 );
);
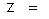 valęncia do elemento;
valęncia do elemento;
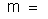 massa de um átomo do elemento;
massa de um átomo do elemento;
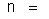 número de íons do elemento que chegam ao eletrodo durante
a eletrólise, e que é igual ao número de átomos depositados;
número de íons do elemento que chegam ao eletrodo durante
a eletrólise, e que é igual ao número de átomos depositados;
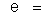 carga elétrica do elétron
carga elétrica do elétron
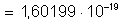 coulombs.
coulombs.
Conforme já
vimos no tópico "Leis
de Faraday sobre a Eletrólise", temos as duas equaçőes:
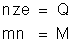
Tiramos:
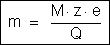
Basta, portanto,
medirmos a massa M do elemento depositado e a carga elétrica Q (o
produto da intensidade da corrente pelo tempo) para sabermos a massa
do átomo.

Massa
do átomo de prata – Sabemos
que uma carga
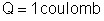 deposita 0,001118 gramas de prata e que a prata é monovalente.
A massa de um átomo de prata é pois:
deposita 0,001118 gramas de prata e que a prata é monovalente.
A massa de um átomo de prata é pois: